Un trauma cranico o lesione cerebrale traumatica (TBI) si verifica quando una forza esterna causa un danno fisico al cervello compromettendone le sue funzioni temporaneamente o permanentemente. I ricercatori dell’Istituto di farmacologia traslazionale del Centro nazionale delle ricerche (Cnr-lft) hanno osservato che la somministrazione precoce per via nasale della molecola della Montalcini, il Nerve Growth Factor (NGF), potrebbe ridurre gli effetti dei traumi cerebrali ed evitare le disabilità motorie. Testato per ora nei modelli animali in futuro potrebbe arrivare nelle sperimentazioni cliniche.
Il trauma cranico è una delle principali cause di morte e dello stato di coma in tutto il mondo ed è responsabile dei danni cerebrali nei bambini e nei giovani. Le cause più frequenti sono gli atti violenti, gli incidenti e le attività sportive. I TBI è causato da una forza meccanica che comporta una frattura del cranio, ematoma ed edema. Oltre a danni causati al momento della lesione, diversi fenomeni si possono verificare nei minuti o nei giorni successivi all’evento traumatico, provocando lesioni secondarie. Questi processi includono alterazioni nel flusso sanguigno cerebrale e della pressione intracranica.
Ad oggi – premettono gli scienziati – il trauma cranico è trattato esclusivamente con terapie palliative che non prevengono o limitano i danni secondari ma sono utili solo a stabilizzare i deficit. Lo studio dei ricercatori del Cnr di Roma, pubblicato sul British Journal of Pharmacology, spiega Marzia Soligo del Cnr-Ift, tra gli autori della ricerca, nasce proprio dall’esigenza di limitare l’insorgenza delle lesioni secondarie, prevenire la morte cellulare indotta dal trauma e quindi contenere lo sviluppo del danno cerebrale, sia nella zona d’impatto che in altre aree del cervello.
Il ruolo dell’NGF
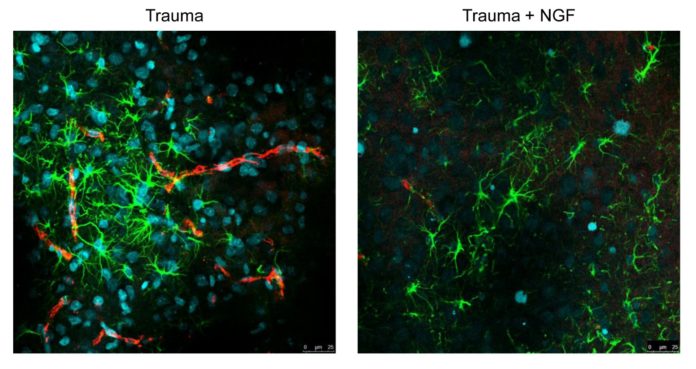
Il Nerve Growth Factor (NGF) o Fattore di Crescita Nervoso è una proteina la cui scoperta valse il premio Nobel a Rita Levi Montalcini nel 1986, coinvolta nello sviluppo del sistema nervoso dei vertebrati e responsabile della crescita degli assoni. La somministrazione intranasale di questa molecola, ad oggi sperimentata solo sei mesi dopo che un trauma cranico aveva compromesso in un bambino le funzioni motorie e cognitive, ha prodotto miglioramenti delle funzioni cliniche e neurologiche. Gli esperti, sulla base di queste conoscenze e tenendo in considerazione che 24 ore dopo un TBI sono già evidenti deficit funzionali, hanno somministrato per via nasale la molecola di NGF a ratti di soli 20 giorni che, per le caratteristiche delle lesioni, potrebbero rappresentare il reale contesto clinico nel trauma cranico nei più piccoli. Il trattamento intranasale con l’NGF ha prevenuto l’instaurarsi di disabilità motorie legate all’equilibrio e alla coordinazione, ha ridotto l’ipertrofia e l’infiammazione. L’NGF è stato somministrato ai ratti immediatamente dopo il trauma. Infatti, già 90 minuti dopo era evidente una assenza di coordinazione motoria, e una sola somministrazione di NGF è stata in grado di limitare la progressione della disabilità.
Le prospettive cliniche
“Benché questo trattamento sia applicato a pazienti con traumi cronici – cioè a distanza di mesi dal trauma – l’aspettativa è che questi dati preclinici possano aprire all’esplorazione degli effetti del trattamento precoce con NGF, da associare alle cure primarie per coloro che hanno appena subito una lesione cerebrale grave”, conclude Luigi Manni, ricercatore del Cnr-flt e primo autore della ricerca. Questi dati preclinici dovrebbero aprire una nuova linea di ricerca orientata verso un trattamento acuto intranasale di NGF e precoce nei bambini ricoverati per trauma cranico grave. Sono però necessari esperimenti dose-risposta per identificare la quantità minima di farmaco che garantisca l’efficacia del trattamento.
Riferimenti: Cnr, British Journal of Pharmacology
Credits immagine: via Cnr